Tirzepatida (Mounjaro) para apneia do sono
Pontos principais do artigo
Nenhuma classe de medicamentos está recebendo mais atenção do que os análogos dos peptídeos intestinais (análogos do receptor do GLP-1 ou análogos combinados GLP-1/GIP).
Esta popularidade é bem justificada: são medicamentos que têm apresentado resultados muito positivos em termos de perda de peso em pessoas com sobrepeso ou obesidade e com efeitos adversos de baixo risco.
Ainda quanto à obesidade, ela possui várias complicações, sendo a síndrome da apneia obstrutiva do sono (SAOS) uma delas.
SAOS é uma das condições que definem a presença de “obesidade clínica”
segundo a nova proposta de critérios diagnósticos
. Trata-se de uma condição em que a pessoa apresenta alterações da fisiologia do sono por episódios frequentes e curtos de pausas respiratórias, levando a hipoxemia.
Na obesidade, este fenômeno é mediado pelo aumento da pressão nas vias aéreas por acúmulo de tecido adiposo na região cervical.
Suas consequências incluem aumento da pressão arterial e do risco de eventos cardiovasculares, bem como comprometimento da qualidade de vida, da capacidade laboral e do desempenho cognitivo.
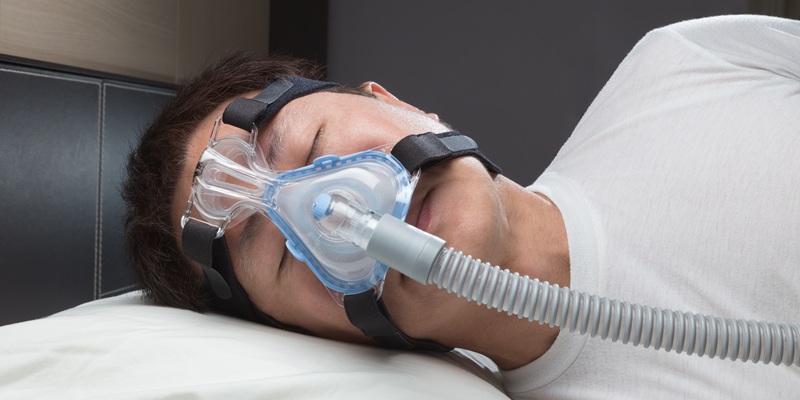
A base do seu tratamento é a redução da obstrução das vias aéreas (através da perda de peso, na maioria das pessoas), suspender o consumo de álcool e sedativos e o uso de equipamentos de pressão positiva (CPAP) nas vias aéreas durante o sono.
Na interface entre obesidade e SAOS, a tirzepatida (Mounjaro®) foi recentemente aprovada pela Agência Nacional de Vigilância Sanitária (ANVISA) para o tratamento de apneia obstrutiva do sono. Esta posição da ANVISA segue a decisão do FDA (órgão dos EUA semelhante à ANVISA) do final de 2024.
Veremos neste texto o que significa esta aprovação, os estudos que a embasam e como isso impacta a prática clínica.
Posição das agências reguladoras
A aprovação do uso da tirzepatida para a indicação de SAOS é significativa, pois trata-se da primeira medicação aprovada especificamente para este fim. Ambas as decisões (tanto da ANVISA quanto do FDA) se baseiam nos resultados de dois ensaios clínicos randomizados publicados
em um mesmo artigo no New England Journal of Medicine em junho de 2024
.
Em sua aprovação, o FDA reforça as preocupações tradicionais com o medicamento:
- Evitar o uso em pessoas com história familiar de câncer medular de tireoide ou com neoplasia endocrina múltipla tipo 2;
- Atentar para o risco de pancreatite, colelitíase e consequente colecistite, hipoglicemia, dano renal, progressão da retinopatia em pessoas com diabetes mellitus tipo 2, alterações comportamentais (inclusive ideação e comportamento suicida) e risco de aspiração durante procedimentos cirúrgicos. Apesar de potencialmente graves, individualmente, todos estes eventos adversos são infrequentes e devem ser discutidos com o médico assistente.
A ANVISA informa que se estima que quase 1,5 milhão de pessoas tenham sido expostas ao medicamento em todo o mundo e que “as notificações com maior frequência nesse período, mas ainda com baixa incidência, foram pancreatite, vômito, diarreia, náusea, desidratação, insuficiência renal aguda.”
Por fim, é importante ressaltar que, no Brasil, o medicamento é aprovado para pessoas com índice de massa corporal (IMC) maior ou igual a 27 kg/m² e alguma complicação da obesidade, incluindo, agora, o SAOS.
Os estudos que embasam a decisão
Os estudos que embasaram a decisão regulatória foram dois ensaios clínicos randomizados, duplo-cego e controlados por placebo, conduzidos em múltiplos centros distribuídos em nove países, com seguimento de um ano.
Do ponto de vista metodológico, são estudos de boa qualidade. A principal deles limitação diz respeito ao uso de um desfecho escolhido: índice de apneia e hipopneia (IAH). É um desfecho amplamente aceito e parece correlacionar-se bem com desfechos mais duros (como morte); entretanto, este não é um desfecho clínico definitivo (tal como morte, eventos cardiovasculares, acidentes de trânsito).
Atentar aos critérios de elegibilidade em um estudo é importante para saber a quem o resultado do estudo se aplica (um dos passos para avaliar a validade externa). Os critérios de inclusão foram semelhantes entre os dois ensaios:
- IAH ≥ 15 eventos por hora;
- Obesidade (IMC ≥ 30 kg/m², ou ≥ 27 no Japão);
- A principal distinção entre os subestudos foi a população incluída quanto ao uso de CPAP. O Subestudo 1 avaliou pessoas que não utilizavam CPAP, seja por preferência pessoal, seja por intolerância, enquanto o Subestudo 2 incluiu participantes que já utilizavam CPAP.
- Os critérios de exclusão incluíram variação autorreferida de peso superior a 5 kg nos três meses anteriores ao recrutamento, planejamento de cirurgia para apneia do sono ou obesidade, diagnóstico de apneia central ou mista e presença de anomalias craniofaciais maiores.
Ambos os estudos utilizaram o mesmo regime de intervenção experimental. A tirzepatida foi iniciada em 2,5 mg por semana, com aumentos de 2,5 mg a cada quatro semanas durante um período de escalonamento até atingir a dose máxima tolerada entre 10 e 15 mg em 20 semanas.
Um aspecto relevante é que todos os participantes, independentemente do grupo ao qual foram alocados (tirzepatida ou placebo), receberam aconselhamento estruturado sobre estilo de vida, incluindo orientação para manter um déficit calórico de 500 kcal por dia e praticar pelo menos 150 minutos de atividade física por semana.
Quanto aos benefícios, o uso de tirzepatida reduziu o número de IAH em mais de 25 eventos por hora (em comparação a uma redução de 5 eventos por hora com placebo). O padrão de redução foi semelhante nos pacientes com e sem uso de CPAP e parece ter sido mediado por uma perda de mais de 15% do peso corporal.
Além disso, houve melhora da pressão arterial, entre -4 e -8 mmHg. Os eventos adversos foram semelhantes aos já conhecidos para a medicação. Aqui, uma comparação é importante: o uso de CPAP reduz o número IAH por ora e pressão arterial em magnitude semelhante.
É interessante notar que, em uma publicação subsequente do mesmo estudo, a tirzepatida também teve benefício em desfechos como qualidade de vida, frequência de sintomas reportados por pacientes avaliados por diferentes escalas de avaliação da doença.
Ou seja, houve redução da fadiga e da sonolência, e aumento da qualidade do sono e da qualidade de vida em geral.
Ainda assim, alguns pontos ficam em aberto, como os efeitos a longo prazo e a sustentação dos resultados com a suspensão do medicamento. Em especial, há curiosidade sobre se essa redução do desfecho substituto (taxa de eventos de apneia e hipopneia) se traduzirá em benefícios cardiovasculares.
Além disso, as preocupações com a segurança de qualquer medicamento relativamente novo no mercado são frequentes e provavelmente serão respondidas com o passar dos anos de uso.
Conclusão: como aplicar isto na prática?
Estes resultados são animadores, uma vez que acrescentam um recurso ao tratamento de pessoas com SAOS por obesidade. A tirzepatida também surge como alternativa para pacientes que não se adaptam ao CPAP.
Deve-se destacar que este é um tratamento caro e que há poucos dados da tirzepatida para esta indicação. Além disso, os efeitos a longo prazo ainda precisam ser avaliados. Em suma, no dia a dia do atendimento a pessoas com obesidade, a presença de SAOS reforça a opção por este medicamento.
