Crise hiperglicêmicas: manejo na emergência
Pontos principais do artigo
As crises ou emergências hiperglicêmicas são o evento final e mais grave que ocorre em pessoas com diabetes
mellitus
(DM), sendo consideradas as principais complicações agudas e que colocam a vida do paciente em risco. Apesar dos esforços para conscientização e diagnóstico, há uma tendência global de aumento na incidência destes eventos na última década. Parte deste aumento foi atribuído à pandemia de COVID-19. Enquanto a cetoacidose diabética (CAD), quando bem tratada, tem mortalidade de menos de 1%, o estado hiperosmolar hiperglicêmico não-cetótico (EHH) tem risco de morte significativamente maior (10-20%) em função do contexto em que ocorre.
Nesta postagem iremos ver o mecanismo destes eventos, bem como seu diagnóstico e manejo na emergência.
Leia também:
Rabdomiólise: o que é e como investigar a causa?
Fisiopatogenia e etiologias
O evento básico é a hiperglicemia desencadeada pela ausência de insulina e pelo aumento dos hormônios contrarregulatórios (glucagon, cortisol). Essa hiperglicemia sustentada ao longo do tempo (usualmente horas a dias para CAD, dias ou semanas para EHH) leva a desidratação e perda de eletrólitos progressivas por perda de água livre pela diurese osmótica. A
Figura 1
resume estes eventos.
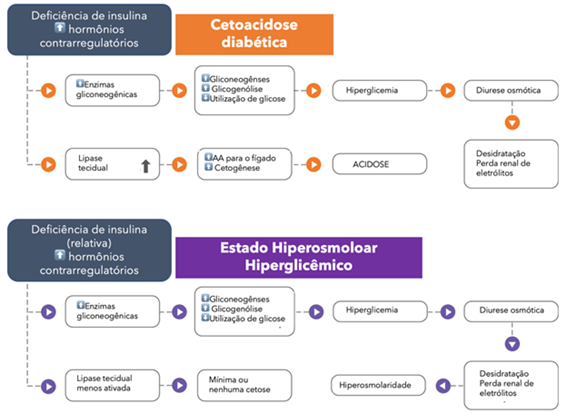
Figura 1.
Sequencia de eventos metabólicos que ocorrem nas crises hiperglicêmicas (cetoacidose diabética e estado hiperosmolar). Extraído e traduzido da referência 2.
Apesar de serem tratadas em conjunto pelas semelhanças no manejo e no processo fisiopatológico, existem algumas diferenças importantes entre a CAD e o EHH. Nenhum dos dois eventos é exclusivo de algum tipo de DM, mas a CAD é típica de pacientes com DM tipo 1, enquanto o EHH é mais frequente em pacientes com DM tipo 2. Na CAD, em função da ausência (quase) completa de insulina, a sequência de eventos leva a marcada produção de cetoácidos, associado assim a desidratação a presença de acidose (
Figura 1
).
Este evento não ocorre no EHH; mas este, por sua vez, tende a ser mais prolongado no tempo e ocorrer em pessoas mais velhas e com mais morbidades. Ou seja, nos pacientes com EHH o grau de desidratação e desequilíbrio eletrolítico é mais intenso, o que explica a seu maior risco de morte.
Quanto à etiologia, os mais diferentes eventos agudos de saúde podem servir de desencadeante. Apesar disso, mais de 70% dos casos são as causados por diagnósticos recentes de DM, omissão de doses de insulina e infecções sistêmicas. Uso de medicamentos como corticóides e antipsicóticos (pela hiperglicemia) e diuréticos (pela desidratação) podem contribuir para o quadro. Mais recentemente, inibidores da enzima SGLT-2 entraram no rol de possíveis desencadeantes de CAD. Isso ocorre por que eles contribuem com a desidratação (pela glicosúria e natriurese), bem como levam a redução da secreção de insulina. Além disso, pelo efeito de controlar a hiperglicemia, estes quadros tendem a cursar sem hiperglicemia (CAD normoglicêmica).
Diagnóstico
O quadro clínico das crises hiperglicêmicas pode envolver uma variedade de sinais e sintomas. Alguns são típicos de hiperglicemia, como poliúria, polidipsia, perda ponderal, enquanto outros são bastante inespecíficos, como náuseas e vômitos, dor abdominal, sonolência. Hipotensão, hipotensão postural e taquicardia são eventos comuns aos dois tipos de emergências hiperglicêmicas, uma vez que marcam a depleção de volume.
A respiração de Kussmaul (um padrão de taquipneia com movimentos ventilatórios longos e profundos) e o hálito cetônico são típicos da CAD. Por outro lado, alterações do sensório (pela hiperosmolaridade) são mais esperadas no EHH.
A investigação inicial de um paciente com suspeita de EHH ou CAD envolve obviamente a realização de glicemia, mas também avaliação de eletrólitos, gasometria, hemograma e investigação de cetose. Vale lembrar que nem toda cetose deve ser encarada como equivalente de CAD, jejum prolongado, consumo de álcool e hiperêmese gravídica são situações que também cursam com elevação de cetonas.
Os critérios diagnósticos de CAD e EHH são facilmente compreendidos e lembrados ao se prestar atenção no nome da das complicações. Como vimos na fisiopatogênese, ambas cursam com desidratação e (tipicamente) hiperglicemia. Na CAD há também
acidose
metabólica por
cetoácidos
, enquanto no EHH há desidratação grave pela
hiperglicemia
levando a
hiperosmolaridade
. Os critérios diagnósticos para ambas condições estão apresentados na
Tabela 1
.
Tabela 1.
Critérios diagnósticos para as crises hiperglicêmicas: cetoacidose diabética e estado hiperosmolar. Extraído e traduzido da referência 1.
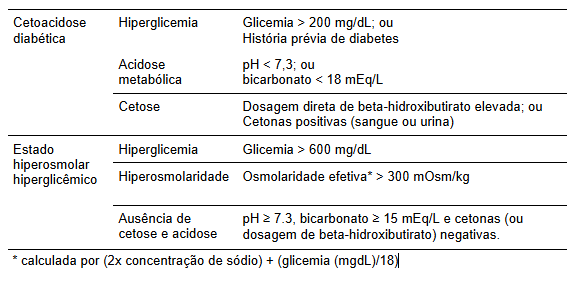
Estes são apresentados em uma diretriz de 2024 e tem algumas pequenas diferenças – porém relevantes – em relação aos critérios mais encontrados na literatura. O nível de glicemia para CAD foi reduzido de 250 mg/dL para 200 mg/dL e foi incluído no critério de hiperglicemia a “história prévia de DM". Ambos foram adicionados para minimizar o risco de omissão de casos de CAD em pessoas com CAD normoglicêmica, que representa aaproximadamente 10% dos casos e está mais comum com o aumento do uso de inibidores da SGLT-2.
Na CAD, além do diagnóstico, é importante definir a gravidade, pois isso tem impacto no prognóstico e no manejo. Os principais marcadores de gravidade são o nóvel do pH e bicarbonato, que estão levemente alterados nos quadros leves, e o sensório não prejudicado. Estes pacientes podem ser tratados em unidades de enfermaria, desde que com monitoramento frequente. Quando o pH cai de 7,2, o bicarbonato se reduz abaixo de 10-15 mEq/L ou há algum grau de sonolência ou confusão, o quadro deve ser considerado pelo menos moderado e unidades com maior observação (intermediária ou UTI) são recomendadas.
Leia mais:
Hipotireoidismo: diagnóstico e manejo
Manejo
O primeiro passo do cuidado de pacientes com emergências hiperglicêmicas, e talvez o mais importante, é conseguir identificar adequadamente o quadro. Por ter manifestações inespecíficas, o médico atendendo situações de emergência deve estar atento a essa possibilidade diagnóstica.
Após fazer o diagnóstico (
Tabela 1
) o manejo agudo se baseia em um tripé de reposição volêmica, correção do desbalanço metabólico com administração de insulina e ajuste dos desequilíbrios eletrolíticos. Ele está esquematizado na
Figura 2
. Destaca-se a importância de postergar o início da infusão de insulina em pacientes hipoglicêmicos na chegada, para evitar aprofundamento do quadro e risco de arritmias ventriculares graves. Além disso, fósforo e bicarbonato só devem ser administrados de forma exógena em situações de depleção grave.
Figura 2.
Manejo agudo resumido das emergências hiperglicêmicas. Adaptado da referência 1.
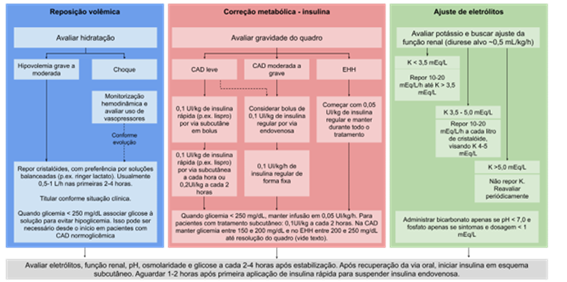
Talvez o erro mais comum no manejo das crises hiperglicêmicas é considerar que a resolução da hiperglicemia permite a suspensão da infusão de insulina. O desequilíbrio metabólico da CAD e do EHH envolve desequiíbrios no metabolismo intermediário que tem um tempo mais protraído para resolução. Isso faz com que, em alguns pacientes, deva-se infundir insulina e glicose de forma concomitante, visando manter a reposição de insulina por mais tempo, sem causar hipoglicemia.
Assim,
a suspensão do uso de insulina contínua e a troca para esquema subcutâneo deve ser realizado quando o paciente estiver em condições de se alimentar por via oral ou enteral e no EHH quando a glicemia estiver abaixo de 250 mg/dL, os eletrólitos e o nível de consciência estiverem normais e o débito urinário acima de 0,5 ml/kg/h. Já na CAD quando a glicemia estiver abaixo de 200 mg/dL e pH estiver acima de 7,3 ou o bicarbonato acima de 18 mEq/L e, se disponível, nível de cetonas abaixo de 0,6 mmol/L.
Aqui cabe um ponto de atenção: na maioria dos serviços não há disponibilidade de dosagem direta de cetonas, mas apenas fita teste com nitroprussiato. Esta opção não é adequada para monitoramento, pois a resolução é sensívelmente posterior à resolução do quadro metabólico.
Por fim, na resolução do quadro, deve-se iniciar insulina subcutânea e, após uma a duas horas da aplicação, suspender a insulina endovenosa. Este período de sobreposição se dá pelo tempo de absorção da insulina subcutânea. Os esquemas de início são os mais variados, desde que contemplem esquemas com insulina bolus e basal.
Uma opção é reiniciar as doses em uso previamente, se houver impressão de que este esquema está correto. Alternativamente, pode-se criar um esquema “do zero", estimando uma dose de 0,5-0,7 UI/kg, conforme o exemplo abaixo para uma pessoa de 70 kg:
- 50% da dose deve ser em insulina basal (NPH, glargina, degludeca): 20 UI pela manhã ou à noite;
- 50% da dose em bolus com insulina rápida (regular, lispro, glulisina), nas 3 principais refeições:
- 4-8 UI no café da manhã, 4-8 UI no almoço e 4-8 UI no jantar;
- Pode-se adaptar as doses para principais refeições (mairo dose nas refeições com maior ingesta de carboidratos);
- Atentar que insulina regular deve ser administrada 30 minutos antes das refeições.
